例谈基于典型问题解决的深度学习
李琛
(南京师范大学附属中学江宁分校 江苏 南京 211102)
摘要:本文以典型问题的解决为突破口,以数学建模为方法,探讨了在澳洲预科大考复习阶段培养学生深度学习、提高复习效率和学生解决问题能力的途径,以期达到复习事半功倍的效果。
关键词:深度学习 典型问题解决 数学建模
一、深度学习的内涵及特征
1、深度学习的内涵
早在 20 世纪中后期,国外学者就展开了对于深度学习 (deep learning)的研究,相对而言,国内有关深度学习的研究起步较晚,直至2005 年,黎加厚等在 《促进学生深度学习》 一文中明确了深度学习的定义,即深度学习是指学习者在理解学习的基础上,批判性地学习新的思想和事实,将它们纳入原有的认知结构中,并且能够联系不同的思想,将已有的知识迁移到新的情境中,做出决策和解决问题的学习。综合国内外对于深度学习概念的阐述,我们可以把深度学习理解为一种主动的、带有批判思维的建构主义学习过程,其目的不是单纯、被动地记忆和理解所学知识,而是能够将新知识与已有知识有效地联系起来,并且能够应用到真实复杂的情境下解决现实存在的问题。
2、深度学习的特征
(1)注重批判性思维的运用。对于所学知识,不能仅停留于“知道”的层面,而在知识的建构过程中,学习者必须批判性地接受所学知识,并对其进行深入思考。只有对该知识有自己充分的理解与看法,才能够算作掌握了所学知识。
(2)强调知识的迁移应用。同一知识点,在不同时间、不同情境甚至不同学科背景下都可能发挥作用。这就要求学习者在批判地理解所学知识的前提下,做到“举一反三”,将所学知识活学活用,而不是机械地记忆。
(3)面向问题的解决。学习的最终目的是解决问题,浅层学习(surface Learning)虽在一定程度上能够解决一部分问题,但更多复杂的实际问题的解决需要以深度学习为基础。“深度”不仅体现在学习过程的主动性与复杂性,更多地反映在问题解决方面。当学习者能够熟练运用某些知识来解决一个现实问题,那他必然对这些知识有充分的理解,并成功地将其综合应用到新的情境中来。因此说问题解决是深度学习的一个重要落脚点。
二、问题解决的内涵及其特征
1、问题解决的内涵
要了解“问题解决”是什么,首先需要明确什么是“问题”。当人们已经掌握了某些已知条件,想要达到某个目标状态,但过程中充满阻碍的时候,问题就产生了。也就是说,问题是个体未能直接达到目标所处的情境 (袁维新等,2010)。依据问题结构性的不同,乔纳森将其分为良构问题和非良构问题。良构问题一般是指已知条件规范、明确,存在有限的正确答案,且有一套完整的解决问题的方法或规则。非良构问题通常与具体情境联系紧密,已知条件模糊,没有明确的解决方法或规则,且答案多呈开放性。通常情况下,我们所说的问题解决主要是针对非良构问题而言。
2、问题解决的特征
(1)情境性。在现实生活中,我们需要解决的常常是不同于课本上结构良好的问题,这就要求我们将学习深度化,利用所学知识、结合具体情境去探索一种全新、合适的解决问题的方法。所以说,问题解决强调“问题”应处于一个真实复杂的情境中。
(2)目标性。一般来说,问题解决都有一个十分明确的目标作为指引,所有的操作活动都是基于目标完成的,也都是为了达成目标。脱离目标的活动不能称作问题解决。
(3)操作序列性。问题解决不是一蹴而就的,它是一个复杂、动态的过程,需要由一系列的心理操作来完成。这些心理操作具有序列性和系统性,不同的 操 作 序 列 形 成 的 解 决 问 题 的 方 法 和 途 径 都 各 不相同。
(4)认知操作性。问题解决是在一定的认知成分基础上展开的,换言之,认知操作是问题解决最基本的成分。如果没有认知成分的参与,只是单纯的一系列有目的性的操作序列,就不能被称为问题解决。
三、数学模型的特征及建构
1、数学建模在化学教学中的必要性
化学学科核心素养中明确要求学生“能认识化学现象与模型之间的联系,能运用多种模型来描述和解释化学现象,预测物质及其变化的可能结果;能依据物质及其变化的信息建构模型,建立解决复杂问题的思维框架。”,可见学会数学建模方法用来解决化学问题应是化学教学追求的目标。
2、数学建模的内涵和建模过程
数学建模方法是把实际问题加以简化、抽象、概括,建立起相应的数学模型,将抽象问题直观化、形象化来研究问题的方法,因而把它运用在化学教学中能起到事半功倍的效果。数学建模的一般过程如下: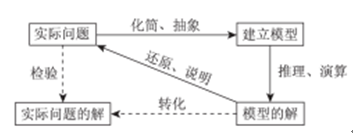
四、基于典型问题解决的深度学习举例
酸碱平衡是新大预科全球大考中的重点内容(每年占比20%左右),也是教学中的难点,如何在复习阶段提高复习效率、提高大考中的得分率,培养学生解决问题的能力一直是我们教学中思考的问题。我们认为如果能结合实际问题、以典型问题的解决为抓手,从而带领学生进入深度学习,对学生能力的培养必能达到事半功倍的效果。为此,我们设计了如下的例题:
Potassium sorbate, KC6H7O2 (molar mass:150g/mol) is commonly added to diet soft drinks as a preservative. A stock solution of KC6H7O2(aq) of known concentration must be prepared. A student titrate 45.00mL the stock solution with1.25M HCl(aq) using both an indicator and a pH meter .The value of Ka for sorbic acid HC6H7O2,is 1.7×10-5.
【问题情境】山梨酸钾作为食品添加剂主要用来防腐,但其在食品中的含量必须控制在安全范围之内,作为研究性学习的主题,测定其含量是一个真实的问题,增强了学习的应用性和兴趣性。
(a)Write the net-ionic equation for the reaction between KC6H7O2(aq) and HCl(aq).
【问题解析】山梨酸钾作为一种弱酸强碱盐水溶液呈碱性,可以与强酸盐酸反应,是一个质子转移反应。
【问题解决】C6H7O2-(aq)+H+(aq)→HC6H7O2(aq)
(b)A total of 30.00mL 1.25M HCl(aq) is required to reach the equivalence point of the titration. Calculate the concentration of KC6H7O2 in the stock solution.
【问题解析】这是一个广义的酸碱中和滴定,根据问题(a)中C6H7O2-与H+的量的关系计算出山梨酸钾的物质的量,进一步求出其浓度。这里的equivalence point是指酸碱恰好完全反应的点(等当量点)。
【问题解决】依据酸碱中和的定量关系:
n(C6H7O2-)=n(H+),
c(KC6H7O2)= c(HCl)×v(HCl)/v(KC6H7O2)
=1.25×30.00×10-3÷(45.00×10-3)
=0.833M
(c)Calculate the pH at the equivalence point of the titration.
【问题解析】在等当量点时,酸碱恰好完全反应,所得溶液是山梨酸和氯化钾的混合溶液,溶液的酸碱性取决于弱酸电离出来的H+的浓度。此时HC6H7O2的浓度为1.25×30.00×10-3÷(75.00×10-3),即0.500M。在已知弱酸的电离常数和浓度时,要求H+浓度,需要借助数学模型进行分析。
【问题解决】
Reaction : HC6H7O2(aq) → C6H7O2-(aq) + H+(aq)
Initial : 0.500 0 0
Change : -x +x +x
Equilibrium : 0.500-x x x
Ka=x2/(0.500-x)= 1.7×10-5
x2= 1.7×10-5×0.500 (x<<0.500M, 0.500-x近似处理后等于0.500)
c(H+)=x=2.915×10-3M
pH=-lg(2.915×10-3)=2.54
(d)Which of the following indicators would be the best choice for determining the end point of the titration? Justify your answer.
【问题分析】中和滴定时指示剂的选择要根据滴定终点(end point)时溶液的pH以及相关指示剂的变色范围,而题给信息中的指示剂的pKa与指示剂的变色范围的关系为:pKa-1~ pKa+1。
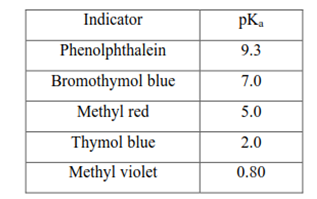
【问题解决】依据表给信息可知选择Thymol blue(百里酚蓝:1.2~2.8,红~黄)是合适的指示剂,滴定终点时的颜色变化为黄色变为橙(红)色。
(e)Calculate the pH at the half-equivalence point.(i.e.The point when the mixed solution behaves like buffer).
【问题分析】the half-equivalence point 是指加入的盐酸恰好一半(15.00mL)时,生成的山梨酸与余下的共轭碱(山梨酸钾)的量相等,实际是等浓度的弱酸及其共轭碱组成的缓冲溶液,HC6H7O2和 C6H7O2-均为1.25×15.00×10-3÷(60.00×10-3)=0.313M。.若求该溶液的pH,也要借助数学建模和电离平衡,此过程中要进行数据的近似处理。
【问题解决】
Reaction : HC6H7O2(aq) → C6H7O2-(aq) + H+(aq)
Initial : 0. 313 0.313 0
Change : -x +x +x
Equilibrium : 0.313-x 0.313+ x x
Ka=(x+0.313)x/(0.313-x)= 1.7×10-5
x= 1.7×10-5M (x<<0.0.313M,0.313-x以及0.313+x近似处理后等于0.313)
c(H+)=x=1.7×10-5M
pH=-lg(1.7×10-5)=4.77
(f) Calculate the pH of the mixture after each of the following volumes of HCl(aq) has been added:
Volume of HCl(aq)/mL | 0.0 | 5.0 | 15.0 | 25.0 | 29.5 | 30.0 | 30.5 | 35.0 |
pH |
【问题分析】本小题求各个时刻的pH均需要首先判断溶液的酸碱性,结合酸的电离或盐的水解,利用数学建模求解,这里只把起点的pH计算过程简单说明(根据酸碱质子理论,C6H7O2-作为质子的接受者,可视作为碱,其水解平衡常数记为Kb,Ka×Kb=Kw)。
【问题解决】
Reaction : C6H7O2-(aq) + H2O (l) → HC6H7O2(aq) + OH-(aq)
Initial : 0.833 0 0
Change : -y +y +y
Equilibrium : 0.833-y y y
Kb=y2/(0. 833-y) = 1.0×10-14/(1.7×10-5)
y= c(OH-)=2.214×10-5M (y<<0.0.0.833M,0. 833-x近似处理后等于0.833)
pOH=-lg(2.214×10-5)=4.65
pH=14-4.65=9.35
(g)Accurately sketch the titration curve on the graph below.Make the position of the half-equivalence point(i.e.The point when the mixed solution behaves like buffer) on the curve with an X.
【问题分析】以问题(f)中所得数据在坐标纸上找点,作出滴定曲线即可。
【问题解决】略
(h)The pH of the solution is 3.37 after the addition of the KC6H7O2(aq).Which species ,HC6H7O2 or C6H7O2-,has a higher concentration in the soft drink ?Justify your answer.
【问题分析】以问题(f)表中的数据分析酸碱中和反应的阶段及粒子的存在形式,列表如下。
滴入盐酸的体积/mL | 0.0 | 15.0 | 30.0 |
溶液的pH | 9.35 | 4.77 | 2.54 |
主要粒子 | C6H7O2- | HC6H7O2 与 C6H7O2-等量 | HC6H7O2 |
【问题解决】根据上表画出数轴,找出pH与粒子存在形式的关系。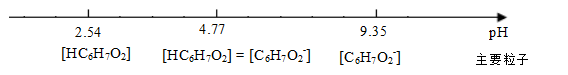
根据题给的pH数据,结合数轴可知,pH为3.37时,[ HC6H7O2]> [ C6H7O2-]。
【教学反思】该典型例题以饮料中防腐剂山梨酸钾的含量测定为情境,综合复习了酸碱中和滴定的计算、指示剂的选择、弱酸的电离、盐的水解、缓冲溶液等不同阶段的pH计算、滴定曲线的绘制,最后进一步探究了特定pH时粒子的存在形式,以问题串的方式复习了酸碱平衡的主要知识点,一条主线、网罗一片,确实具备典型问题的要件,也完全符合问题解决的主要特征。如果我们的教学中经常进行类似的设计,学生的问题解决能力和深度学习的能力必定会有明显的提高。
参考文献
【1】张立国等,基于问题解决的深度学习模型[J],中国远程教育,2017(8):27-33
【2】汤礼志,数学建模在化学探微教学中的应用初探[J],教育导刊,2000(6)上半月刊:35-37
【3】徐凯里,建模思想在化学原理教学中的应用[J],化学教育,2018年第39卷17期:32-37
【4】大连理工大学无机化学教研室,高等教育出版社,无机化学第四版[M]:136-137

